ISP ordena retiro voluntario de relajante muscular inyectable por riesgo de partículas de vidrio

La autoridad sanitaria solicitó detener de inmediato el uso del lote XP1T1 de Mivacron, tras detectar fallas en el control de partículas que podrían provocar lesiones graves en pacientes.
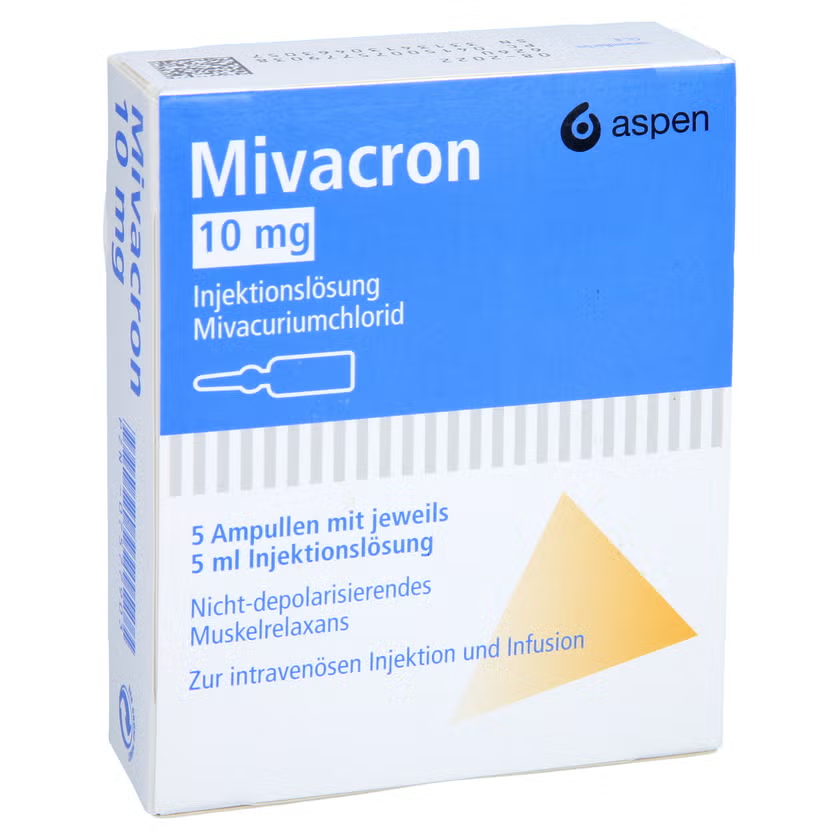
El Instituto de Salud Pública (ISP) instruyó el retiro voluntario de un lote específico del relajante muscular inyectable Mivacron Solución Inyectable 10 mg/5 mL, fabricado por Aspen Chile, luego de identificar un fallo en el sistema de inspección visual que podría permitir la presencia de trozos de vidrio al interior de las ampollas. La advertencia fue emitida como una medida inmediata de seguridad para centros asistenciales y profesionales de la salud.
El relajante muscular, cuyo principio activo es mivacurio, se utiliza durante procedimientos anestésicos para facilitar la intubación y la ventilación mecánica. El lote afectado corresponde a la serie XP1T1, con registro sanitario F-26587/22 y fecha de vencimiento al 30 de octubre de 2027. Según el ISP, su uso debe ser suspendido por completo debido a los potenciales efectos adversos de inyectar partículas extrañas en el torrente sanguíneo.
Entre las complicaciones descritas por la autoridad se incluyen flebitis, obstrucciones en la circulación, embolias, necrosis tisular, riesgo de sepsis y daño en órganos vitales como pulmones, riñones o hígado. Estas reacciones se producen por la respuesta inflamatoria que generan los fragmentos de vidrio al ingresar al organismo.
Para los establecimientos que aún posean unidades del lote XP1T1, el ISP ordenó tres pasos críticos:
- No utilizar el producto bajo ninguna circunstancia.
- Segregar inmediatamente las unidades existentes para evitar su uso accidental.
- Devolverlas al titular del registro, Aspen Chile, siguiendo los canales habituales de distribución.
La alerta puede complementarse con material gráfico del envase afectado, cápsulas de audio explicando los riesgos asociados a partículas contaminantes en inyectables y un video informativo sobre cómo los servicios de salud deben ejecutar procesos de retiro voluntario. Además, es útil incluir una sección interactiva que oriente a los farmacéuticos sobre protocolos de reporte, registro y control de estos incidentes.
El ISP reiteró que este tipo de retiros permite actuar preventivamente ante fallas que pueden comprometer la seguridad de los pacientes, especialmente en medicamentos administrados en contextos críticos como pabellones quirúrgicos y unidades de cuidados intensivos.